皆さん、こんにちは。
ベトナム、ホーチミンの川村 拓己です。
【質問】
日本からベトナムへ医療機器を輸出し、ベトナムの病院(市場)へ販売を行いたいです。
進出検討段階なのですが、事前に考慮すべきことなどございますでしょうか。
【回答】
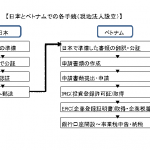
今回は医療機器のベトナムでの販売における注意点をご紹介いたします。
前回のブログで、医療機器の輸出入を行うためには製品をベトナムの保険局に申請、登録をする必要がある旨ご紹介させていただきました。
製品を販売する場合も同様に、輸出入とは別に申請、登録する必要がございます。
政令36/2016, 169/2018 / ND-CPの第17条によりますと、
製品が輸出入の規制に従っているだけでなく、製品の情報がラベルに詳細に記載されるのかどうか、修理やメンテナンスのための必要なマニュアルを用意しているかどうか、ベトナム語で取扱書を作成しているかどうかなど別途規制が課されております。
Article 17. Requirements for registration of medical devices
1. Any medical devices to be registered and placed on the market must satisfy the following requirements:
a) Having an effective registration number or having obtained permission for import according to provisions of this Decree;
b) Having label or supplementary label containing sufficiently information specified in Article 54 of this Decree;
c) Having technical documents serving the repair and maintenance of medical devices, excluding disposable medical devices prescribed by its owner;
d) Having Vietnamese instruction of how to use the medical devices;
dd) Having information about warranty establishments, conditions and duration, unless the device is disposable as decided by its owner.
2. The information specified in points c, d and dd clause 1 of this Article, which is not enclosed with the device, must be provided in form of electronic information; guidelines for accessing to such information must be clearly stated on the label of the medical devices.
外資系の医療関係製品のベトナム市場への参入がまだ少なく、法律のみならず、当局の判断も明確ではないため、輸入から販売の許可を取るまでにはかなりの時間が要すると考えられます。
株式会社東京コンサルティングファーム ベトナム ホーチミン拠点
川村 拓己
Mail: kawamura.hiroki@tokyoconsultinggroup.com
※)記載しました内容は、作成時点で得られる情報をもとに、最新の注意を払って作成しておりますが、その内容の正確性及び安全性を保障するものではありません。該当情報に基づいて被ったいかなる損害についても情報提供者及び当社(株式会社東京コンサルティングファーム並びにTokyo Consulting Firm Co., Ltd.)は一切の責任を負うことはありませんのでご了承ください。